Biophysique cellulaire

Responsable d'équipe
Notre équipe interdisciplinaire étudie les mécanismes de délivrance de molécules dans les cellules et les tissus en utilisant des champs électriques et des systèmes basés sur les nanoparticules. Notre objectif est d’améliorer le ciblage et la délivrance des agents thérapeutiques, ainsi que de mieux diagnostiquer les lésions cancéreuses. Nous utilisons des modèles de complexité croissante, allant des liposomes aux cellules, organoïdes et souris. Grâce à divers outils d’imagerie avancée, nous cherchons à visualiser, comprendre et optimiser les processus de perméabilisation des membranes et des cellules à différentes échelles.
Notre équipe réunit une expertise interdisciplinaire pour améliorer les méthodes de délivrance non-virale, ouvrant la voie à des stratégies innovantes pour combattre le cancer ainsi que les infections bactériennes et les complications associées.

Au cours des 30 dernières années, notre groupe a développé une approche multidisciplinaire combinant la biologie cellulaire et la biophysique pour élucider les mécanismes des perturbations membranaires induites par les modifications du potentiel transmembranaire, spécifiquement à travers les techniques d’ « électroporation » ou d’ « électroperméabilisation ». Nos recherches ont ouvert la voie à des approches innovantes et établi des paramètres pour une délivrance sans risque et efficace de molécules thérapeutiques dans les cellules et les tissus.
Nos recherches s’articulent autour de plusieurs thématiques :
- Élucidation des Mécanismes d’Électrotransfert : Nos études ont révélé les processus distincts impliqués dans le transfert de molécules thérapeutiques (telles que la bléomycine et le cisplatine), de petits oligonucléotides (siARN et LNA), de protéines et de plasmides d’ADN. Ces mécanismes ont été étudiés in vitro à l’aide de modèles cellulaires 2D et 3D, ainsi qu’in vivo chez des modèles murins.
- Développement des Techniques d’Électroporation : Nos recherches ont conduit à la création de nouveaux types de générateurs d’impulsions électriques et d’électrodes, adaptés aux études in vitro et in vivo. Nous avons également adapté des systèmes d’imagerie, y compris des chambres à fenêtre dorsale et des microscopies/macroscopies à fluorescence, pour visualiser les processus biologiques se déroulant lors de l’électroporation pour le traitement du cancer et l’éradication des pathogènes.
- Exploration des Approches de Délivrance de Médicaments Non-Viraux : Nous étudions des méthodes alternatives de délivrance de médicaments non-viraux, telles que les transporteurs à base de lectines qui ciblent spécifiquement les cellules cancéreuses pour la délivrance ciblée des agents thérapeutiques et le diagnostic, ainsi que des nanoparticules inorganiques capables d’exercer des actions physiques locales pour détruire les tumeurs solides, les bactéries et les biofilms.
- Étude des Effets Biologiques des Radiofréquences : Nous investiguons les effets biologiques des radiofréquences, y compris celles utilisées dans les réseaux de télécommunication 5G, pour déterminer les éventuels effets sur la santé que les radiations électromagnétiques pourraient avoir sur les systèmes vivants.
Nous collaborons activement avec plusieurs réseaux internationaux, notamment le Consortium International de Bioélectrique, le Réseau Européen pour le Développement des Technologies et Traitements Basés sur l’Électroporation, et le LIA-EBAM : Laboratoire International Associé sur les Applications des Champs Électriques Pulsés en Biologie et Médecine. Nous collaborons également avec des chercheurs internationaux, cliniciens et partenaires industriels qui développent des dispositifs d’électroporation. Nous sommes actuellement impliqués dans trois projets européens. Deux d’entre eux, les projets ETAIN et GOLIAT, portent sur l’étude des effets potentiels sur la santé de l’exposition aux champs électromagnétiques, y compris le 5G. Le troisième projet, ZAPcancer, se concentre sur les effets de la mort cellulaire immunogène sur l’activation de la réponse immunitaire antitumorale, induite par l’électrochimiothérapie.
Équipe
Chercheurs-Enseignants chercheurs
Maxime Berg (CR, CNRS)
Muriel Golzio (DR2, CNRS)
Jelena Kolosnjaj-Tabi (CR, CNRS)
Laurent Paquereau (PR1, UPS)
Marie-Pierre Rols (DR CE, CNRS)
Techniciens et ingénieurs
Geraldine Alberola (IE, CNRS)
Elisabeth Bellard (IR1, CNRS)
Laetitia Hellaudais (ADTRF1, UPS)
Caroline Ladurantie (TCE, CNRS)
Franck Talmont (IR HC, CNRS)
Ophélie Cordier
Post-Doctorants
Coralie Cayron
Georgios Kougkolos
Doctorants
Nicolas Mattei
Emma Barrere
Nos projets de recherche (en anglais)
de Caro et al. (2025) New effective and less painful high frequency electrochemotherapy protocols: From optimization on 3D models to pilot study on veterinary patients. J Control Release
Kralj et al. (2025) Dynamically assembling magnetic nanochains as new generation of swarm-type magneto-mechanical nanorobots affecting biofilm integrity. Adv Healthc Mater
Kolosnjaj-Tabi et al. (2021) High Power Electromagnetic Waves Exposure of Healthy and Tumor Bearing Mice: Assessment of Effects on Mice Growth, Behavior, Tumor Growth, and Vessel Permeabilization. Int J Mol Sci
Coustets et al. (2020) Development of a near infrared protein nanoprobe targeting Thomsen-Friedenreich antigen for intraoperative detection of submillimeter nodules in an ovarian peritoneal carcinomatosis mouse model. Biomaterials
Kolosnjaj-Tabi et al. (2019) Electric field-responsive nanoparticles and electric fields: physical, chemical, biological mechanisms and therapeutic prospects. Adv Drug Deliv Rev
Pasquet et al. (2019) Pre-clinical investigation of the synergy effect of interleukin-12 gene-electro-transfer during partially irreversible electropermeabilization against melanoma. J Immunother Cancer
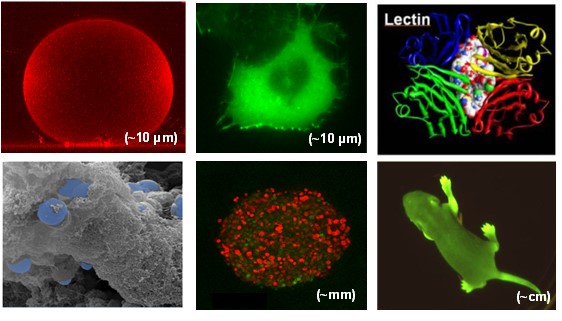
Biological systems of increasing complexities to unravel the mechanisms of drug delivery and improve cancer treatment and diagnosis. We use pulsed electric fields, macromolecules and nanoparticle-based systems. © Cellular biophysics group
See English version
See English version
See English version

