Comment les lymphocytes T font la distinction entre des antigènes d’affinités différentes
Les lymphocytes T sont des cellules essentielles du système immunitaire, et ont la capacité de détecter un large éventail de peptides antigéniques liés au complexe majeur d’histocompatibilité (CMH). Pourtant, ils ne déclenchent une réponse appropriée qu’après avoir reconnu des antigènes de haute affinité provenant d’agents pathogènes, tandis que l’interaction avec des peptides du soi ne les active pas. Grâce à une analyse phosphoprotéomique et interactomique approfondie et résolue dans le temps des événements de signalisation qui se produisent dans les cellules T lors de la stimulation avec des peptides d’affinité différente, les scientifiques de l’IPBS et du CIML ont déchiffré les mécanismes qui régissent cette discrimination hautement spécifique. Ces résultats sont publiés dans la revue Nature Immunology.
L’activation, la différenciation et la réponse phénotypique des lymphocytes T dépendent de la spécificité et de la force des signaux délivrés par le récepteur des cellules T (TCR) lors de la reconnaissance d’un peptide antigénique. Bien que des auto-peptides de faible affinité dérivés de protéines de l’hôte puissent se lier au TCR, ils ne déclenchent pas de réponse, même s’ils sont présents à une concentration élevée. À l’inverse, même de petites quantités de peptides antigéniques étrangers qui se lient au TCR avec une forte affinité suffisent à activer pleinement les lymphocytes T. Pour atteindre une telle spécificité, il a été postulé que le TCR utilise un mécanisme de vérification cinétique, basé sur la présence de multiples étapes intermédiaires biochimiques entre la liaison à l’antigène et une étape finale irréversible conduisant à une activation complète. Cela introduit un délai qui permet uniquement aux antigènes de haute affinité, qui restent liés au TCR suffisamment longtemps, de compléter la série d’étapes de signalisation conduisant à l’activation des cellules T.
La stimulation du TCR favorise la phosphorylation rapide et successive de nombreuses protéines intracellulaires, ainsi que des interactions protéine-protéine et la formation de complexes. Afin de caractériser plus en détail ces mécanismes, et d’identifier les étapes clés de la discrimination antigénique, les scientifiques ont analysé de manière globale tous les événements moléculaires qui se déroulent dans les cellules T lorsque le TCR est engagé à l’aide de ligands peptidiques d’affinités décroissantes. Ils ont appliqué des approches basées sur la spectrométrie de masse pour suivre la cinétique de phosphorylation de plusieurs milliers de protéines, et la formation de complexes autour de différentes molécules importantes de la voie de signalisation.
Ils ont ainsi pu classer de manière non biaisée les événements indépendants de l’affinité du ligand, ceux présentant une réponse s’échelonnant avec l’affinité du ligand, et ceux provoqués uniquement par des ligands forts. Certains événements moléculaires en amont ne semblent pas du tout affectés par les différences d’affinité des ligands, par exemple la phosphorylation des chaînes CD3 du TCR et le recrutement de la kinase ZAP70 au TCR. Les différences entre les ligands forts et les ligands faibles sont plutôt reflétées par des changements dans l’étape finale de trans-autophosphorylation du domaine catalytique de ZAP70, requise pour l’activation complète de la kinase, et dans la formation du signalosome LAT, qui est sévèrement altérée avec les ligands faibles. L’assemblage du signalosome CD6 n’est que partiellement affecté, et il contient encore des molécules inhibitrices qui pourraient jouer un rôle dans l’atténuation des signaux TCR dans des conditions de stimulation avec des ligands de faible affinité.
Cette étude fournit des connaissances fondamentales sur la manière dont la série d’étapes de signalisation en aval du TCR joue un rôle dans la discrimination antigénique, conformément au modèle de relecture cinétique. Ces connaissances sur les mécanismes de signalisation du TCR pourraient être utiles à l’avenir pour la conception rationnelle de récepteurs chimériques de cellules T utilisés pour l’immunothérapie anticancéreuse. Elle fournit également une ressource de données utile pour les chercheurs, en révélant de nouvelles molécules candidates qui pourraient jouer un rôle dans la voie du TCR.
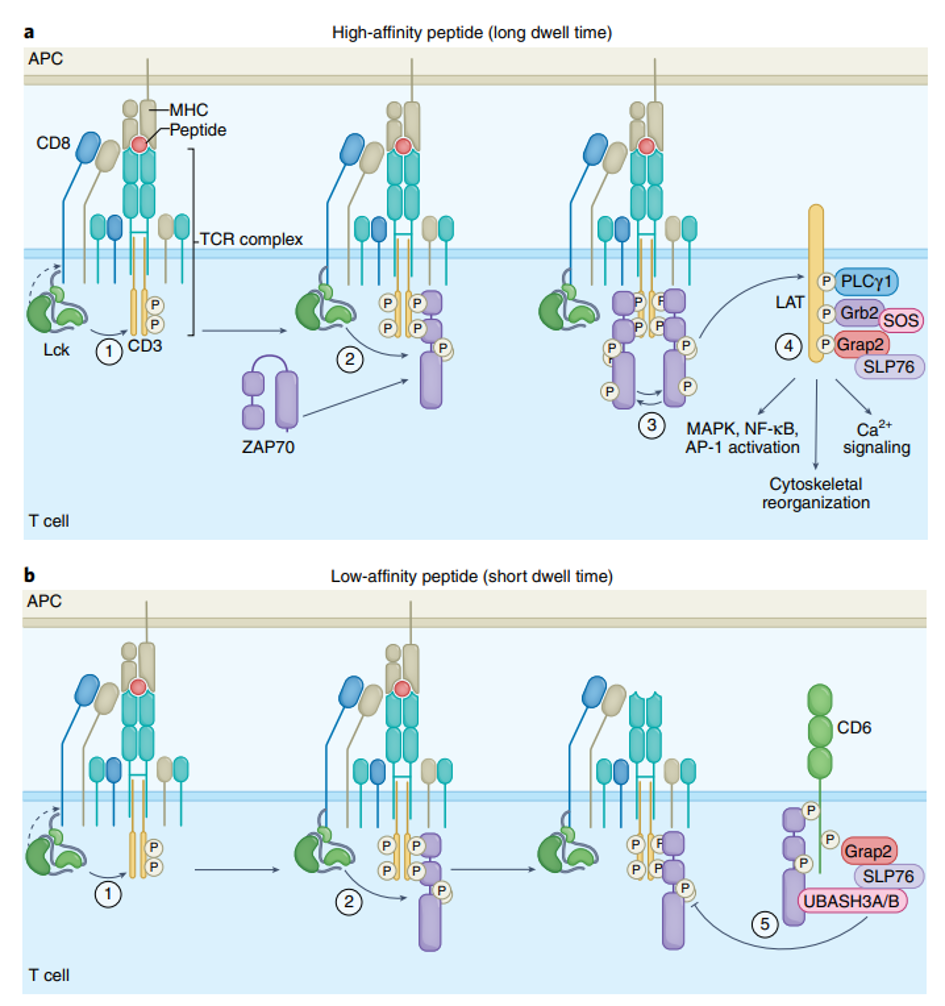
La signalisation du récepteur des cellules T est déclenchée lorsque le TCR se lie à un peptide antigénique lié au CMH, conduisant à la phosphorylation des chaînes CD3 et au recrutement de la kinase ZAP70.
(a) La stimulation avec des ligands de haute affinité permet de compléter toutes les étapes de la phosphorylation de ZAP70, conduisant à l’activation complète de la kinase et à la formation du signalosome LAT, orchestrant la réponse des cellules T.
(b) Par contre, lorsque le TCR se lie à un peptide de moindre affinité présenté par le CMH, la demi-vie de l’interaction n’est pas assez longue pour permettre à l’étape 3 de l’activation de ZAP70 d’avoir lieu. La stimulation avec des peptides faibles permet seulement la formation du signalosome CD6, qui est capable d’entraîner une boucle de rétroaction négative
Source
“Kinetic proofreading through the multi-step activation of the ZAP70 kinase underlies early T cell ligand discrimination”
Voisinne, G., Locard-Paulet, M., Froment, C., Maturin, E., Menoita, M.G., Girard, L., Mellado, V., Burlet-Schiltz, O., Malissen, B.*, Gonzalez de Peredo, A.*, and Roncagalli, R.*
Nature Immunology, August 13 2022
Contact Chercheur
Anne Gonzalez de Peredo | gonzalez@ipbs.fr
Contact Presse
Françoise Viala
communication@ipbs.fr | +33 (0)6 01 26 52 5

